Rodanidi kaalium on toksiline aine, mida kasutatakse analüütilistes keemiates
Potassium Rodanid( vastavalt IUPAC-i kaasaegsele nomenklatuurile - kaaliumtiotsüanaat) - kristallid, millel ei ole värvi ja lõhna;peenelt hajutatud olekus nad omandavad valge värvuse. Aine on mõru terav maitse, mürgine. Kaaliumduraniid on paljudes lahustites nagu vesi, amüülalkohol ja etanool lahustuv.
omandamine Aine saadakse ainult keemiliselt, see ekstraheeritakse looduslikest allikatest( veri ja inimese sülg) - väga kallis. Kaaliumtiotsüanaadi sünteesiks on vaja segada ammooniumtiotsüanaadi ja kaaliumhüdroksiidi lahuseid( triviaalne nimetus - kausid).
Katse tehakse veojõu all, kuna vabanev ammoniaak võib põhjustada keemilisi põletusi ja mürgitust;Seejärel filtreeritakse puhastatud lahus ja jääk aurustatakse, et saada soovitud aine kristallid. Kui toode vabaneb 70% -ni ja piisavalt puhas ammooniumtiotsüanaadi proov, on see meetod väga tõhus.

Teine meetod on väävlit sulandada kaaliumtsüaniidiga, kuid see meetod kaaliumtiotsüanaadi saamiseks on tsüaniidi kõrge toksilisuse tõttu väga ohtlik.
Kasutatakse
Kaaliumtiotsüanaati, selle derivaate ja erinevate kontsentratsioonidega lahuseid mitmes tööstuses. Näiteks:
- Tekstiilitööstus.
- Film foto.
- Orgaaniline süntees.
- Analüütiline keemia.

- kasutusalad tekstiilitööstuses. Kaaliumtiotsüanaadi lahust kasutatakse kangaste, näiteks siidi, riide värvimiseks ja töötlemiseks, et säilitada materjali algupäraseid omadusi.
- orgaanilises sünteesis. Mõningad orgaanilised ained, nagu tiouurea, sünteetilise sinepiõli ja mitmesugused värvained, sünteesitakse kaaliumtiotsüanaadist. Selle abiga saadakse ka teisi tiootsüanaate, näiteks vasktiotsüanaati-2.
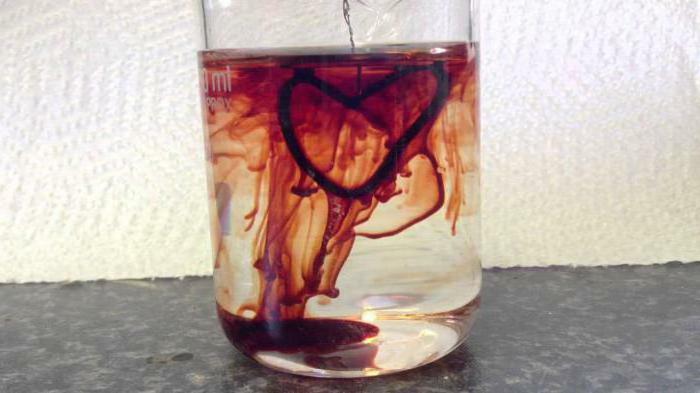
- Analüütilises keemias kasutatakse kaaliumtiotsüanaadi lahust, et määrata aine ferri raa katioonid. Illustreeriv näide on reaktsioon, milles kaasatakse ka kaaliumtiotsüanaati ja raud-3-kloriidi, mida nimetatakse ka "veri veest", milles moodustub karmisonist punane heksatsüanoferraat 3;Triviaalne nimi on punane vere sool. Samuti kasutatakse tiotsüanaate, et eraldada haruldasi metalle nagu toorium ja lantaan. Kaaliumdudaniid ja raudkloriid on hiljuti aidanud kaasa filmimiseks tehisvere saamiseks, kuid see meetod läheb taustale, kuna filmitööstuses on arvutigraafika kasutusele võtmine.
- Põllumajanduses on tiootsüanaatide lahustest saadav tugev insektitsiid. On kaks võimalikku reaktsiooni:
- Esimene on tiotsüanuurhappe produktsioon, eemaldades kaaliumist soola;Rodan on kõigi elusorganismide jaoks üsna ohtlik gaas ja seda kasutatakse harva.
- Teine on kaaliumtiotsüanaadi lahustamine, hüdrolüüsil vabanenud vesiniktsüaniidhappe kogumine ja saadud aine oksüdeerimine tsüanogeeniks. Tsüaan pole süstlaga võrreldes vähem mürgine, kuid raskem, ja seetõttu kasutatakse seda sageli insektitsiidina.
Potassium rodanide on toksiline aine, mille surmav annus on suu kaudu manustamisel umbes 0,9 grammi aine kohta kehakaalu kilogrammi kohta.
Kättesaadavus
Rodanidi kaaliumit saab osta mis tahes keemias, kuid väikestes kogustes suure toksilisuse tõttu. Reaktiivi keskmine hind on nelisada rubla kilogrammi kohta, enamasti piirdub müük ühes käes kahele kilogrammile.
Turvalisus
Mürgisuse tõttu tuleb kaaliumtiotsüanaati säilitada erinõuete kohaselt ohutusnõuete täitmiseks mürgiste ainete käitlemisel:
- kristalle ja kaaliumtiotsüanaadi on rangelt keelatud suukaudselt ja on äärmiselt ebasoovitav sissetungimist lahendusi kõrges kontsentratsioonis põhiainet nahale.
- Vaatamata sellele, et ravim on mürgine ainult määruse sissepoole töö sisu on soovitav kummikindaid kitlit, ja nagu kõik kemikaalide ohutuse põhinõuded.
- peaks isoleerida aine lapsed ja isikud, kellel ei ole teadmisi laboris, sest see võib põhjustada ebameeldivaid juhtumeid kaotuse reaktiivid, väärkasutuse ja äkksurm.
- Kuna mittesüttiva ainega ja piisavalt stabiilne õhus, on võimalik hallata ladustamise aine pimedas.kuiv kappVältida kõrge õhuniiskus ja otsene päikesevalgus, kui võib juhtuda tõttu reaktiivi halvenemise lagunemine selle osa. Ka Standardi NFPA 704 Orthorhombic märgistamisel tuleb järgmisi sümboleid: 3 0 0 W, kusjuures 3( sinise lozenge) - toksilisuse, 0( punase ja kollase) - süttivuse ja reaktsioonivõime ja W - kaubamärk interaktsiooniks veegamis on toksilise tiotsüaniinhappe vabanemine.
Ja pidage meeles, et keemilised eksperimendid on hämmastavad ja ainulaadsed, kuid mitte kunagi ei võta arvesse ohutusmeetodeid!
